4月24日,威尼斯886699生命科学学院刘忠华/王加强团队与多单位研究人员紧密合作,在Nature核心子刊《Nature Structural & Molecular Biology》上发表题为“Alternative splicing of CARM1 regulated by LincGET-guided paraspeckles biases the first cell fate in mammalian early embryos”的研究论文,该论文揭示了RNA可变剪接调控小鼠第一次细胞命运决定的新机制。
哺乳动物的第一次细胞命运决定是发育生物学领域最基础、最核心的科学问题之一。自从2007年nature文章首次报道H3R26me可以作为4-细胞单卵裂球异质性的marker ,越来越多的证据表明CARM1的分子异质性是导致小鼠第一次细胞命运决定的核心机制——受到CARM1正调控的SOX2/OCT4-SOX21轴促使胚胎走向内细胞团命运,而受到CARM1负调控的BAF155-keritin-CDX2轴促使胚胎走向滋养外胚层命运。2018年2篇cell背靠背文章证明LincGET和paraspeckle可以通过调控CARM1影响第一次细胞命运决定。然而,人们对于CARM1的分子异质性究竟是如何建立的,仍然知之甚少。
为了解析小鼠2-细胞至4-细胞时期CARM1分子异质性形成的机制,研究人员对大量的RNA-seq数据进行了深入分析,发现了一个在小鼠2-细胞和4-细胞中非常特异的现象——编码CARM1核心功能域的外显子3至外显子6存在非常明显的异常外显子跳跃剪接现象。研究人员发现,CARM1的分子异质性来源于3至6号外显子跳跃剪接的异质性,而与转录水平无关。为了进一步探索CARM1可变剪接异质性形成的机制,研究人员对参与可变剪接调控以及细胞命运决定的LincGET和亚细胞核结构paraspeckle进行了研究。结果发现,LincGET参与早期胚胎特异的paraspeckle的组装,并通过与HNRNPU的互作将paraspeckle定位到Carm1的基因座上,抑制Carm1的外显子跳跃剪接。此外,通过对Carm1内含子序列的分析,团队发现PCBP1参与的splicing speckle能够特异性地促进Carm1的外显子跳跃剪接。也就是说,LincGET参与的paraspeckle与PCBP1参与的splicing speckle竞争性调控Carm1的外显子跳跃剪接,造成了Carm1可变剪接水平的异质性。最后,研究人员证明通过过表达PCBP1增强Carm1可变剪接水平的异质性,能够促使卵裂球走向滋养外胚层命运。
该工作不仅揭示了小鼠第一次细胞命运决定中分子异质性形成的机制,还证明了亚细胞核结构的竞争性能够参与细胞决策。该工作为早期胚胎发育和细胞命运决定等基础研究提供了新的见解和方向。
威尼斯886699为第一完成单位,王加强教授为本文第一作者兼共同通讯作者,博士研究生张轶伟和硕士研究生高嘉泽参与了该文章的生信分析工作,博士研究生李鹏程参与了部分实验工作。该文章得到了中国科学院战略性先导科技专项、国家重点研发计划、国家自然科学基金、黑龙江省省自然科学基金等的大力资助和支持,同时得到了威尼斯886699引进人才启动经费的大力支持。
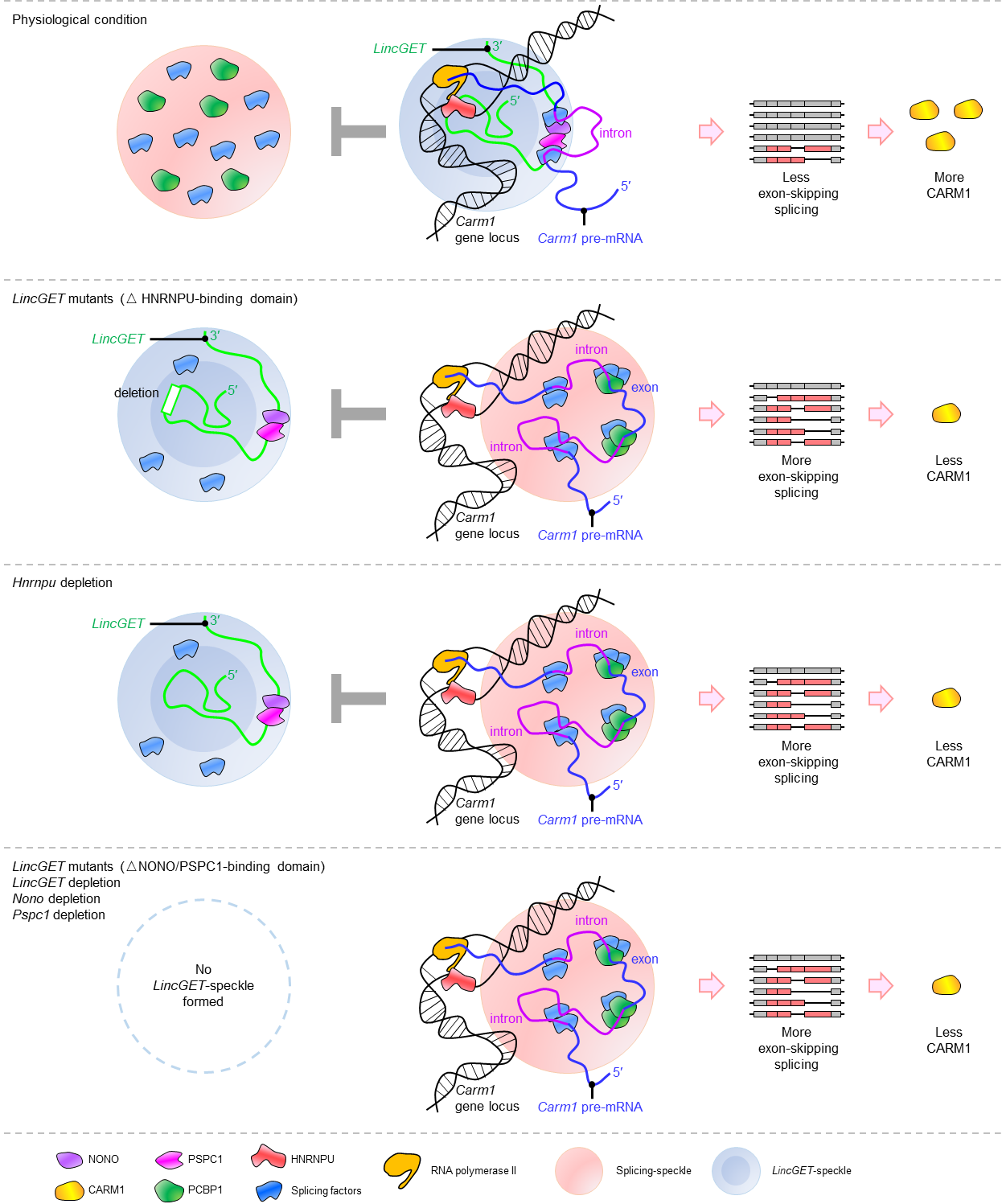
Carm1 外显子跳跃剪接造成CARM1的分子异质性
原文链接:
https://www.nature.com/articles/s41594-024-01292-9
(供稿/生命科学学院)



